بیماری هیرشپرونگ
چیست؟
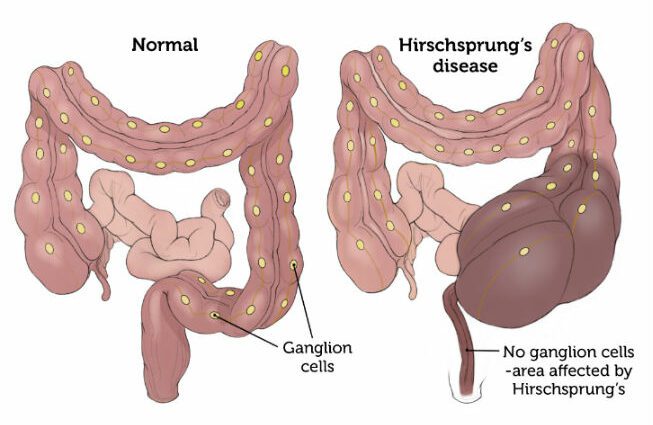
بیماری هیرشپرونگ (HSCR) با فلج در قسمت انتهایی روده بزرگ مشخص می شود.
این آسیب شناسی از بدو تولد ظاهر می شود و نتیجه عدم وجود گانگلیون های عصبی (سلول هایی که در مسیر عصب برآمدگی ایجاد می کنند) در دیواره روده است.
بلع غذا از طریق دستگاه گوارش تا زمانی که دفع نشود ، تا حد زیادی به لطف پرستالیز روده امکان پذیر است. این peristalsis مجموعه ای از انقباضات ماهیچه های روده است که باعث پیشروی بولوس غذا در طول دستگاه گوارش می شود.
در این وضعیت که در گانگلیون های عصبی در روده بزرگ وجود ندارد ، پرستالیز دیگر توسط بدن ارائه نمی شود. به این معنا ، اتساع روده و افزایش حجم آن ایجاد می شود.
اگر ناحیه گانگلیون های عصبی بزرگ باشد علائم مربوطه اهمیت بیشتری پیدا می کند. (1)
بنابراین این بیماری با علائم روده ای غیرمعمول تعریف می شود: انسداد روده. این انسداد گذر و گاز است که منجر به درد شکم ، قولنج (گرفتگی روده) ، تهوع ، نفخ و غیره می شود.
HSCR تقریباً از هر 1 تولد 5 نفر در سال را تحت تأثیر قرار می دهد. شکلی که قسمت انتهایی روده بزرگ (روده بزرگ) را تحت تأثیر قرار می دهد عمدتا پسران را درگیر می کند. (000) دختران بیشتر در معرض توسعه این بیماری به شکل گسترده تری هستند. (2)
این آسیب شناسی بیشتر نوزادان و کودکان خردسال را تحت تأثیر قرار می دهد. (3)
اشکال مختلفی از بیماری نشان داده شده است (2):
-شکل "کلاسیک" یا "شکل قطعه کوتاه" نیز نامیده می شود. این فرم بیشتر در بیماران مبتلا به این آسیب شناسی ، تا 80 شایع است. این شکل از بیماری قسمت انتهایی روده بزرگ را به بخش راست روده مبتلا می کند.
-فرم "بخش طولانی" ، که تا کولون سیگموئید گسترش می یابد ، تقریباً 15 of از بیماران را تحت تأثیر قرار می دهد.
- شکل "قولنج کل" ، که روی روده بزرگ تأثیر می گذارد ، 5 concerns از بیماران را درگیر می کند.
نشانه ها
ترانزیت روده توسط سیستم عصبی کنترل می شود. بنابراین گانگلیون های عصبی در روده قرار دارند که به انتقال اطلاعات از مغز برای کنترل پرستالیز روده و در نتیجه پیشرفت غذا در طول دستگاه گوارش کمک می کند.
عدم وجود این گره ها ، در مورد بیماری هیرشپرونگ ، از هرگونه انتقال اطلاعات جلوگیری می کند و در نتیجه پرستالیز روده را مسدود می کند. غذا دیگر نمی تواند از روده ها عبور کند و در نهایت در دستگاه گوارش مسدود می شود.
علائم این بیماری معمولاً در اوایل تولد قابل مشاهده است. با این حال ، در برخی موارد ، آنها می توانند بعد از یک یا دو سال ظاهر شوند. (3)
علائمی که بر نوزادان تازه متولد شده و کودکان تأثیر می گذارد عبارتند از:
- مشکلات حمل و نقل ؛
- ناتوانی در دفع مکونیوم (اولین مدفوع نوزاد) در 48 ساعت اول ؛
- یبوست؛
- زردی ؛
- استفراغ ؛
- اسهال ؛
- درد شکم ؛
- سوءتغذیه
علائمی که بر کودکان بزرگتر تأثیر می گذارد عبارتند از:
- یبوست شدید با عوارض (عدم رشد در قد و وزن) ؛
- تغذیه نامناسب ؛
- اتساع شکم ؛
- تب.
همچنین ممکن است کودک دچار عفونت های روده ای مانند انتروکولیت شود.
ناهنجاری های اضافی نیز ممکن است قابل مشاهده باشد: کاهش شنوایی حسی عصبی (سندرم واردنبورگ شاه) ، ناتوانی ذهنی (سندرم موات ویلسون) ، هیپوونتیلاسیون مرکزی آلوئول (سندرم حداد) ، ناهنجاری اندام (سندرم باردت) بیدل) ، سرطان تیروئید مدولاری (غدد درون ریز متعدد) نئوپلازی نوع 2B) یا ناهنجاری های کروموزومی (سندرم داون). (2)
منشاء بیماری
بیماری هیرشپرونگ ناشی از ناهنجاری در توسعه سیستم عصبی روده است. این یک آگانگلیونوز است ، یعنی عدم وجود گانگلیون عصبی (که به آن "سلولهای کاجال" نیز گفته می شود) در روده ها. این نقص غدد لنفاوی بیشتر در قسمت انتهایی روده بزرگ (روده بزرگ) قرار دارد.
در موضوعی که تحت تأثیر این آسیب شناسی قرار گرفته است ، بنابراین این قسمت از روده در حالت انقباض مقوی و دائمی باقی می ماند. این وضعیت منجر به انسداد روده می شود. (2)
عوامل ژنتیکی و محیطی در ایجاد بیماری هیرشپرونگ دخیل هستند. (2)
در واقع ، ژنهای خاصی در توسعه این پاتوژنز نشان داده شده است. این یک بیماری پلی ژنتیکی است که به ویژه ژنها را درگیر می کند:
- Proco-oncogene ret (RET) ؛
-ژن عامل نوتروتروفیک مشتق از سلول گلیال (GDNF) ؛
- ژن گیرنده اندوتلین نوع B (EDNRB) ؛
- ژن اندوتلین 3 (EDN3) ؛
- ژن آنزیم تبدیل کننده اندوتلین 1 (ECE1) ؛
- ژن مولکول چسبندگی L1 (L1CAM).
عوامل خطر
همانطور که قبلاً نیز گفته شد ، بیماری هیرشپرونگ نتیجه عدم وجود گانگلیون عصبی در روده بزرگ تا مقعد است و از ایجاد پرستالیز روده جلوگیری می کند و بنابراین غذا به این سطح صعود می کند.
این کمبود سلولهای کاجال (گانگلیون عصبی) نتیجه نقص در رشد این سلولها در طول رشد جنین است. علل این عدم رشد سلولی قبل از تولد هنوز مشخص نیست. با وجود این ، احتمال وجود رابطه بین سلامت عمومی مادر در دوران بارداری و عدم وجود این نوع سلول ها در جنین مطرح شده است.
ژنهای زیادی در ایجاد این بیماری نشان داده شده است. وجود این ژنها می تواند در یک خانواده مکرر باشد. سپس بخشی از وراثت در منشاء توسعه این بیماری خواهد بود.
علاوه بر این ، آسیب شناسی های خاص نیز می توانند یک عامل خطر اضافی از نظر توسعه بیماری هیرشپرونگ باشند. این امر به ویژه در مورد سندرم داون صادق است. (3)
پیشگیری و درمان
تشخیص افتراقی با توجه به علائم مشخصه بیماری ارائه شده توسط فرد انجام می شود: انسداد روده ، تنگی آنورکتال ، تومورهای لگن و غیره (2)
تشخیص اغلب با این بیماری از طریق بیوپسی رکتوم انجام می شود. این بیوپسی وجود یا عدم وجود گانگلیون عصبی در روده بزرگ را نشان می دهد. علاوه بر این ، بیان بیش از حد استیل کولین استراز (آنزیمی که به استیل کولین اجازه می دهد تا به اسید استیک و کولین هیدرولیز شود). (2)
تنقیه باریم (بررسی اشعه ایکس برای تجسم روده بزرگ) نیز می تواند در تشخیص این آسیب شناسی انجام شود. این روش امکان تجسم یک منطقه گذرا از عدم وجود سلول های عصبی را فراهم می کند که نشان دهنده پیشرفت بیماری هششپرونگ است. با این حال ، این روش تشخیصی 100 reliable قابل اعتماد نیست. در واقع ، 10 تا 15 درصد موارد بیماری هیرشپرونگ پس از این تلاش تشخیصی تشخیص داده نمی شود. (4)
مهمترین درمان این بیماری جراحی است. این اجازه می دهد قسمتی از روده که سلول های عصبی کم دارد ، برداشته شود. (4)
در صورت آسیب کلی به روده بزرگ ، ممکن است پیوند روده ضروری باشد. (2)
به دنبال آن ، استومی (تکنیک جراحی که امکان برقراری ارتباط بین دو اندام را فراهم می آورد) را می توان به منظور اتصال قسمت عمل شده روده با مقعد یا قسمت فوقانی روده انجام داد. این روزنه بسته به مورد می تواند دائمی یا موقت باشد. (4)
جراحی به کاهش علائم مرتبط با بیماری کمک می کند. با این حال ، پیش آگهی کامل نیست و عوارض التهابی می تواند ظاهر شود و کشنده باشد.