فهرست
درمان ژنتیکی
استفاده از ژن به عنوان دارو: این ایده پشت ژن درمانی است. استراتژی درمانی شامل اصلاح ژن ها برای درمان یک بیماری، ژن درمانی هنوز در مراحل ابتدایی است، اما اولین نتایج آن امیدوارکننده است.
ژن درمانی چیست؟
تعریف ژن درمانی
ژن درمانی شامل اصلاح ژنتیکی سلول ها برای پیشگیری یا درمان بیماری است. این بر اساس انتقال یک ژن درمانی یا یک کپی از یک ژن عملکردی به سلول های خاص، با هدف ترمیم یک نقص ژنتیکی است.
اصول اصلی ژن درمانی
هر انسان از حدود 70 میلیارد سلول تشکیل شده است. هر سلول حاوی 000 جفت کروموزوم است که از یک رشته مارپیچ شکل دوتایی به نام DNA (دئوکسی ریبونوکلئیک اسید) تشکیل شده است. DNA به چند هزار بخش تقسیم می شود، ژن، که ما حدود 23 نسخه از آنها را حمل می کنیم. این ژنها ژنوم را میسازند، یک میراث ژنتیکی منحصربهفرد که توسط هر دو والدین منتقل میشود، که حاوی تمام اطلاعات لازم برای رشد و عملکرد بدن است. ژن ها در واقع نقش هر سلول را در ارگانیسم نشان می دهند.
این اطلاعات به لطف یک کد، ترکیبی منحصر به فرد از 4 پایگاه نیتروژنی (آدنین، تیمین، سیتوزین و گوانین) که DNA را تشکیل می دهند، ارائه می شود. DNA با کد، RNA را می سازد، پیام رسان حاوی تمام اطلاعات مورد نیاز (به نام اگزون) برای تولید پروتئین ها، که هر کدام نقش خاصی در بدن دارند. بنابراین ما ده ها هزار پروتئین ضروری برای عملکرد بدن خود تولید می کنیم.
بنابراین، تغییر در توالی یک ژن، تولید پروتئین را تغییر می دهد، پروتئینی که دیگر نمی تواند نقش خود را به درستی ایفا کند. بسته به ژن مربوطه، این می تواند منجر به طیف گسترده ای از بیماری ها شود: سرطان ها، میوپاتی ها، فیبروز کیستیک و غیره.
بنابراین، اصل درمان این است که به لطف یک ژن درمانی، یک کد صحیح ارائه شود تا سلول ها بتوانند پروتئین فاقد آن را تولید کنند. این رویکرد ژنی ابتدا شامل شناخت دقیق مکانیسم های بیماری، ژن درگیر و نقش پروتئینی است که برای آن کد می کند.
کاربردهای ژن درمانی
تحقیقات ژن درمانی بر بسیاری از بیماری ها متمرکز است:
- سرطان ها (65 درصد تحقیقات فعلی)
- بیماری های تک ژنی، یعنی بیماری هایی که تنها یک ژن را تحت تأثیر قرار می دهند (هموفیلی B، تالاسمی)
- بیماری های عفونی (HIV)
- بیماری های قلبی عروقی
- بیماری های نورودژنراتیو (بیماری پارکینسون، بیماری آلزایمر، آدرنولوکودیستروفی، بیماری سانفیلیپو)
- بیماری های پوستی (اپیدرمولیز بولوزا پیوندی، اپیدرمولیز بولوزا دیستروفیک)
- بیماری های چشمی (آب سیاه)
- و غیره.
بیشتر آزمایشها هنوز در مرحله تحقیقات فاز I یا II هستند، اما برخی از آنها قبلاً به بازاریابی داروها منجر شدهاند. این شامل:
- Imlygic، اولین ایمونوتراپی انکولیتیک علیه ملانوما، که مجوز بازاریابی (مجوز بازاریابی) خود را در سال 2015 دریافت کرد. از ویروس هرپس سیمپلکس-1 اصلاح شده ژنتیکی برای آلوده کردن سلول های سرطانی استفاده می کند.
- Strimvelis، اولین درمان مبتنی بر سلولهای بنیادی، مجوز بازاریابی خود را در سال 2016 دریافت کرد. این دارو برای کودکان مبتلا به آلمفوسیتوز، یک بیماری نادر ایمنی ژنتیکی (سندرم بچه حبابدار) در نظر گرفته شده است.
- داروی Yescarta برای درمان دو نوع لنفوم غیر هوچکین تهاجمی نشان داده شده است: لنفوم سلول B منتشر منتشر (LDGCB) و لنفوم سلول B بزرگ اولیه مدیاستن مقاوم به درمان یا عودکننده (LMPGCB). مجوز بازاریابی خود را در سال 2018 دریافت کرد.
ژن درمانی در عمل
رویکردهای متفاوتی در ژن درمانی وجود دارد:
- جایگزینی یک ژن بیمار، با وارد کردن کپی یک ژن عملکردی یا "ژن درمانی" به سلول هدف. این را می توان در هر دو حالت in vivo انجام داد: ژن درمانی مستقیماً به بدن بیمار تزریق می شود. یا در شرایط آزمایشگاهی: سلول های بنیادی از نخاع گرفته می شوند، در آزمایشگاه اصلاح می شوند و سپس دوباره به بیمار تزریق می شوند.
- ویرایش ژنومی شامل ترمیم مستقیم جهش ژنتیکی در سلول است. آنزیمهایی که نوکلئاز نامیده میشوند، ژن را در محل جهش قطع میکنند، سپس بخشی از DNA ترمیم ژن تغییر یافته را ممکن میسازد. با این حال، این رویکرد هنوز فقط تجربی است.
- اصلاح RNA، به طوری که سلول یک پروتئین کاربردی تولید می کند.
- استفاده از ویروس های اصلاح شده به نام انکولیتیک برای از بین بردن سلول های سرطانی.
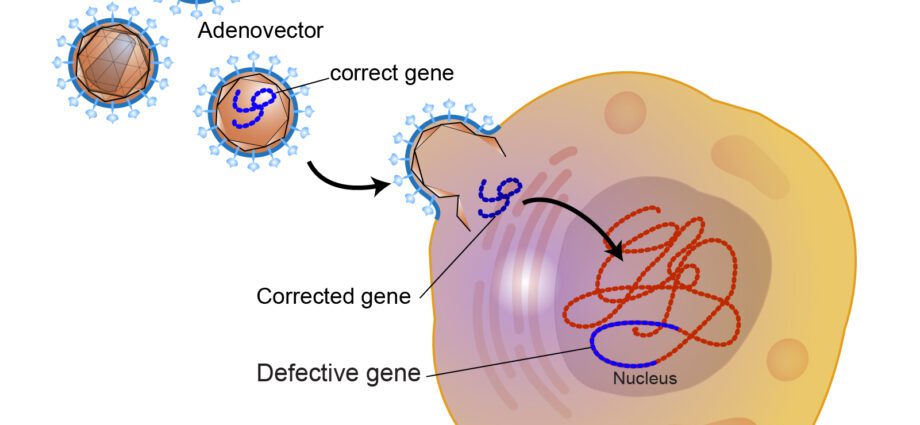
برای رساندن ژن درمانی به سلول های بیمار، ژن درمانی از به اصطلاح ناقل استفاده می کند. آنها اغلب ناقلان ویروسی هستند که پتانسیل سمی آنها لغو شده است. محققان در حال حاضر روی توسعه ناقل های غیر ویروسی کار می کنند.
تاریخچه ژن درمانی
در دهه 1950 بود که به لطف شناخت بهتر ژنوم انسان، مفهوم ژن درمانی متولد شد. با این حال، چندین دهه طول کشید تا اولین نتایج به دست آید، که ما آن را مدیون محققان فرانسوی هستیم. در سال 1999، آلن فیشر و تیمش در اینسرم موفق به درمان "حباب های نوزاد" شدند که از نقص ایمنی ترکیبی شدید مرتبط با کروموزوم X (DICS-X) رنج می بردند. این تیم در واقع موفق شده است یک نسخه طبیعی از ژن تغییر یافته را با استفاده از یک ناقل ویروسی نوع رتروویروس در بدن کودکان بیمار وارد کند.